谁在控制你的饭量?Nature新发表论文:肠道细菌才是真正的指挥官
在人体肠道中,数万亿微生物与我们形成了精妙的共生关系。但长久以来,这些微小生命如何实时影响宿主行为却始终是个谜。
在人体肠道中,数万亿微生物与我们形成了精妙的共生关系。但长久以来,这些微小生命如何实时影响宿主行为却始终是个谜。
8月6日,《自然》杂志发表了杜克大学研究院团队夫的重大发现:一种前所未有的“神经生物感知”系统(neurobiotic sense),揭示了肠道微生物通过特定分子模式与大脑直接对话的奥秘——结肠细胞能快速检测微生物蛋白质,并立即向大脑发送抑制食欲的信号。这一突破或将彻底改变我们对肠道微生物影响行为、情绪甚至心理健康的认识。



杜克大学医学院的研究团队聚焦在位于结肠上皮细胞内一种名为“神经足”的微型传感器细胞。神经足细胞在肠道上皮细胞中的占比很小,但是却拥有惊人的感知能力,它们能检测常见微生物蛋白质,并向大脑快速传递信号,帮助抑制食欲。
但这仅仅是个开始。研究团队认为,这种“神经生物感知”可能是一个更广阔的研究平台,将帮助人们理解肠道如何感知微生物,进而影响从饮食习惯到情绪状态等各个方面,甚至大脑如何反过来塑造微生物组。
“我们好奇的是,身体是否能实时感知微生物模式——不仅是作为免疫或炎症反应,而是作为一种能实时指导行为的神经反应。”该研究资深作者、杜克大学医学院医学与神经生物学教授Diego Bohórquez解释道。
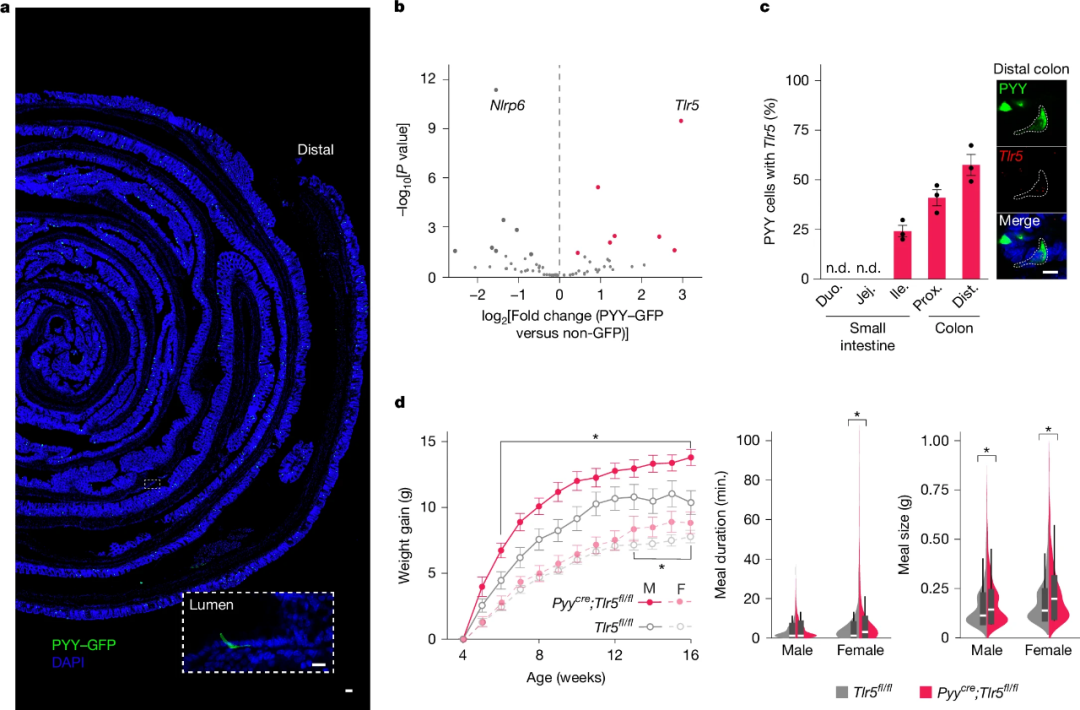
结肠PYY标记细胞中微生物模式识别受体TLR5的缺失增加了食物摄入量
这项研究的关键在于鞭毛蛋白,这是一种存在于细菌鞭毛(细菌用来游动的鞭状结构)中的古老蛋白质。当我们进食时,一些肠道细菌会释放鞭毛蛋白。神经足细胞通过TLR5受体检测到这种蛋白质后,会通过迷走神经(肠道和大脑之间的一条主要通讯线路)向大脑发送信息。
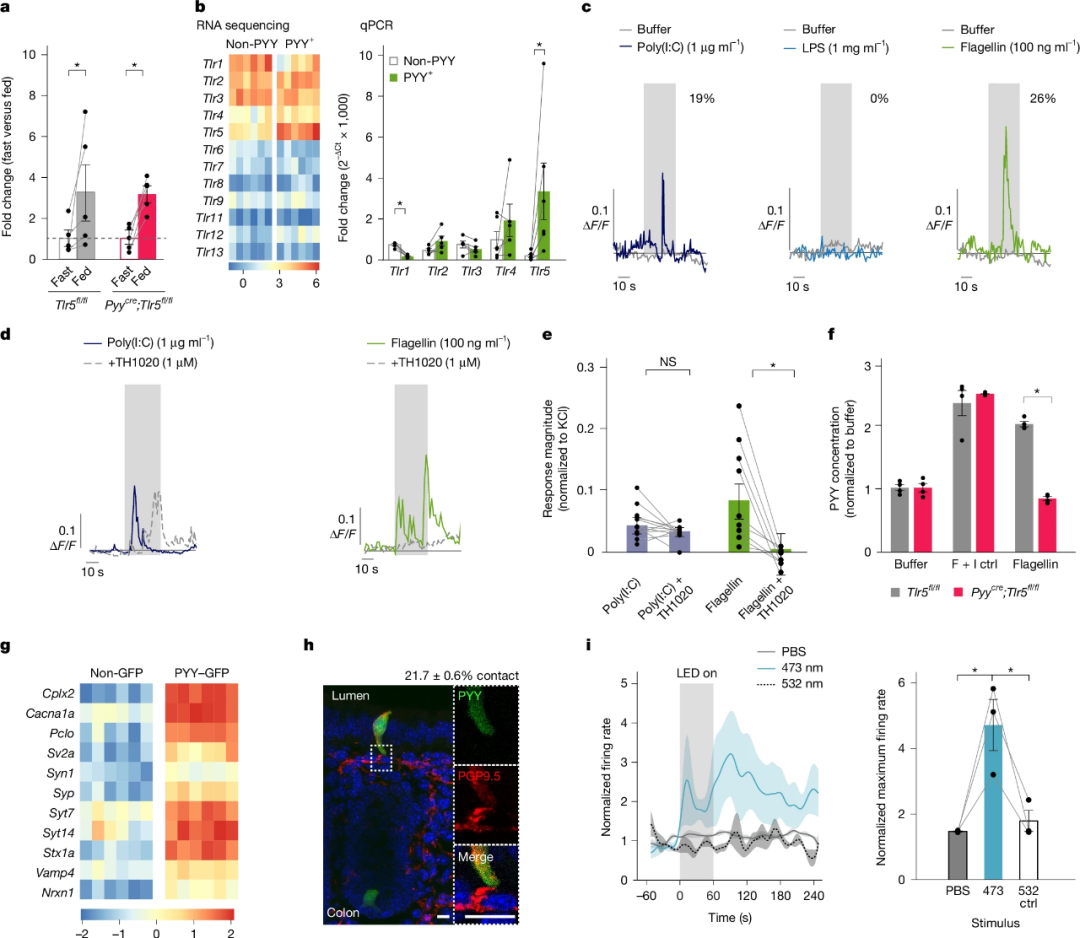
PYY标记的细胞通过TLR5感知微生物鞭毛蛋白
在美国国家卫生研究院支持下,研究团队提出了一个大胆假设:结肠中的细菌鞭毛蛋白可能触发神经足细胞向大脑发送抑制食欲的信号——这是微生物直接影响行为的直接证据。
研究人员通过禁食小鼠实验验证了这一假设:当向小鼠结肠直接给予小剂量鞭毛蛋白后,它们的食量明显减少;而在缺乏TLR5受体的小鼠身上进行同样的实验时,则未观察到任何变化,这些小鼠持续进食并且体重增加。这一结果表明,该通路有助于调节食欲。

研究结果表明,鞭毛蛋白通过TLR5发送“已经吃够了”的信号,让肠道告知大脑该停止进食了。如果没有这种受体,信号就无法传递。
研究团队通过实验证明,破坏这一通路会改变小鼠的饮食习惯,这揭示了肠道微生物与行为之间存在更深层次的联系。
这项开创性研究不仅揭示了肠道与大脑之间惊人的实时对话机制,更为开发针对代谢性疾病和精神健康障碍的新型干预策略提供了可能。随着科学界对“神经生物感知”系统的深入探索,我们或将迎来通过调控肠道微生物来改善整体健康的新时代。
“这为理解微生物如何影响人类行为打开了新窗口,下一步明确的研究方向是探究特定饮食如何改变肠道微生物群落,这可能成为解开肥胖或精神障碍等疾病谜题的关键一环。”Bohórquez表示。